Glykogen střádající choroba II neboli Pompeho choroba je autosomálně recesivní dědičná porucha metabolismu u laponských ovčáků a švédských a finských laponských psů. Dysfunkce enzymu α-1,4-glukosidáza přítomného v lysozomech má za následek narušení degradace glykogenu, který se na základě toho hromadí v buňkách. Vše vyúsťuje v poškození převážně svalů, srdce a jater. Nemoc je pro psy fatální, terapie neexistuje.
Glykogen střádající choroby (glycogen storage disease, GSD), také glykogenózy, patří mezi vrozená metabolická onemocnění, která můžeme najít u lidí, ale i u různých plemen psů. Příčinou těchto dědičných vad je nepřítomnost či nefunkčnost enzymů nebo transportních proteinů v těle, které hrají důležitou roli v metabolismu glykogenu. Pokud kvůli chybějícímu enzymu nedochází k úplnému odbourávání glykogenu, pak se začne ukládat v různých orgánech, převážně v játrech a svalech, ale také v ledvinách a srdci. Toto ukládání je potom příčinou patologických stavů (myopatie, hepatopatie atd.). Rozlišujeme několik typů glykogen střádajících chorob, podle toho, který protein/enzym je nefunkční.
Tento článek pojednává o glykogen střádající chorobě II (Pompeho choroba, GSD II) způsobené nefunkčností enzymu α-1,4-glukosidáza, který v lysozomech hraje důležitou roli při biochemickém štěpení glykogenu na glukózu. Jedná se tedy zároveň o poruchu metabolismu lysozomů. Tato dědičná a často fatální nemoc byla popsána u plemen finský laponský pes, laponský ovčák a švédský laponský pes a můžeme ji srovnat s infantilní formou Pompeho choroby u lidí.
Na úvod
Co je to lysozom? Každá savčí buňka má v sobě několik organel, malých tělísek, přičemž každá má svoji specifickou funkci. Jednou z nich je i lysozom, jehož funkce je pohlcovat do sebe velké molekuly (např. proteiny, tuky, sacharidy), a rozbíjet je na malé fragmenty, které mohou být buňkou dále snadněji zpracovány. K tomuto fragmentování slouží různé enzymy, které jsou v lysozomech uloženy. Pokud je jen jediný enzym nefunkční, chybí nebo má omezenou funkci, dojde k hromadění a ukládání těchto látek, určených původně „k recyklaci“, v buňkách. Tato nechtěná zásoba uvnitř buňky může být ale pro buňku fatální a může dojít až k jejímu zániku. V případě Pompeho choroby se v lysozomech ukládají velké molekuly glykogenu, které nemohou být odbourány na glukózu, a to má za následek poškození buněčných funkcí.
Glykogen je polysacharid složený z několika tisíc molekul glukózy, které jsou navzájem pospojovány (α-1,4 a α-1,6 glykosidovými vazbami) tak, že výsledkem je bohatě větvená struktura glykogenu. Glykogen je velice důležitý zásobní sacharid, jenž slouží jako zdroj energie hlavně v období hladovění nebo fyzické práce, prostě v případech, kdy v krvi poklesne hladina glukózy. Jaterní buňky pojímají největší zásobu glykogenu, méně potom buňky svalové. Glykogen ve svalech slouží jako místní energie pro svalovou činnost a ten uložený v jaterních buňkách se po přeměně na glukózu (glykogenolýza) dostává do krve. V lysozomech je přítomný enzym α-1,4-glukosidáza, zvaný také kyselá maltáza, který štěpí α-1,4 a α-1,6 glykosidové vazby glykogenu, maltózy a isomaltózy. α-1,4-glukosidáza má v lysozomu za úkol štěpit glykosidové vazby mezi glukózami tak, aby došlo k rozbití větvené struktury glykogenu až na jednotlivé molekuly glukózy.
Monosacharid glukóza je nejdůležitějším a nejrychlejším zdrojem energie pro živočišný organismus. Hladinu glukózy v krvi udržuje buď její transport ze střeva do krve po příjmu potravy, nebo její tvorba přímo v organismu, buďto již zmíněnou glykogenolýzou anebo novotvorbou glukózy z různých substrátů (glukoneogenezí).
Jaké jsou klinické projevy této nemoci?
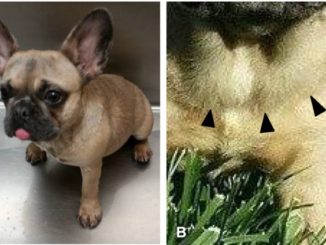
Klinické příznaky nemoci se nezačnou projevovat hned po narození, ale až u několika měsíčních štěňat (7 – 12 měsíců). Prvotním projevem nemoci je nejčastěji zvracení hlenu nebo regurgitace a ztráta kondice. Při podrobném vyšetření je možné zjistit příčinu zvracení a regurgitace. Tou je tzv. megaesophagus neboli rozšíření jícnu. Jak dochází k poškození svalů ukládáním glykogenu, trpí psi svalovou slabostí, která se stále zhoršuje. Majitelé si u psů všímají také ztíženého dýchání (dyspnoe) a lapání po dechu. Při vyšetření hrudníku se zjišťuje zvětšení srdce (kardiomegalie).
Co je příčinou této dědičné vady?
Enzym α-1,4-glukosidáza je kódován genem GAA. U lidí bylo objeveno několik set možných mutací tohoto genu, které vedou k Pompeho chorobě. U psů dochází kvůli mutaci genu GAA k úplné dysfunkci enzymu, což má za následek hromadění glykogenu v lysozomech a k následnému poškození svalové tkáně, ale také jiných tkání a orgánů jako jater, ledvin a srdce. Toto poškození vyúsťuje ve svalovou slabost a srdeční a dýchací potíže, které nakonec vedou ke smrti pacienta.
U psů se jedná o autosomálně recesivní dědičnou vadu, stejně jako je u lidí infantilní forma Pompeho choroby. Klinické příznaky způsobené úplnou ztrátou funkčnosti enzymu α-1,4-glukosidáza se projeví u zvířat, která od každého z rodičů získala po jedné recesivní alele, která nese kopii defektního genu. Aby tedy nemoc u psa propukla naplno, musí mít dvě tyto recesivní alely (p/p). Pokud ale potomek zdědí mutovanou kopii genu pouze po jednom z rodičů (P/p), označuje se jako heterozygot neboli skrytý nosič nemoci. U takovýchto zvířat se neprojeví žádné klinické příznaky onemocnění, ale můžou přenášet mutaci genu na další generace. Tabulka ukazuje pravidla autosomálně recesivní dědičnosti při křížení dvou jedinců.
| KŘÍŽENÍ DVOU JEDINCŮ | P/P | P/p | p/p |
| P/P (zdravý) | 100% zdravé potomstvo | 50% zdravého potomstva, 50 % potomstva budou nosiči | 100% potomstva budou nosiči |
| P/p (nosič) | 50% zdravého potomstva, 50 % potomstva budou nosiči | 25% zdravého potomstva, 50% potomstva budou nosiči, 25% potomstva bude postiženo GSD II | 50% potomstva budou nosiči, 50% potomstva bude postiženo GSD II |
| p/p (GSD II) | 100% potomstva budou nosiči | 50% potomstva budou nosiči, 50% potomstva bude postiženo GSD II | 100% potomstva postiženo GSD II |
Jak zjistím, že můj pes trpí glykogen střádající chorobou?
Diagnostický test prokazující přítomnost mutace genu GAA pro enzym α-1,4-glukosidáza je dostupný jak pro chovatele tak majitele laponských psů. Odběr vzorku (krev, sliny) pro tento test DNA je snadno proveditelný a psího pacienta nijak nezatěžuje. Cílem tohoto testování je nejen odhalit pravou diagnózu, ale hlavně skryté nosiče nemoci a zabránit tak jejich nekontrolovanému využití v chovu, při kterém hrozí, že mutovaný gen zdědí i část potomstva. Pokud bychom vyřadili všechny nosiče z chovu, dá se teoreticky nemoc vymýtit.
Existuje terapie?
Léčba tohoto vzácného metabolického defektu u psů zatím bohužel neexistuje. Pokud dříve nedojde k úhynu pacienta, přistupuje se, vzhledem k progresivitě nemoci a snížené kvalitě života, k eutanázii.
Reference:
- Seppälä EH, Reuser AJJ, Lohi H (2013) A Nonsense Mutation in the Acid α-Glucosidase Gene Causes Pompe Disease in Finnish and Swedish Lapphunds. PLoS ONE 8(2): e56825. https://doi.org/10.1371/journal.pone.0056825
- Wikipedia, The Free Encyclopedia, Glycogen, WWW.: < https://en.wikipedia.org/wiki/Glycogen>
- Juvenilní laryngeální paralýza a polyneuropatie - 21 července, 2021
- Exokrinní pankreatická insuficience (EPI) - 20 července, 2020
- Hypertyreóza u koček - 6 července, 2020




Buďte první kdo přidá komentář